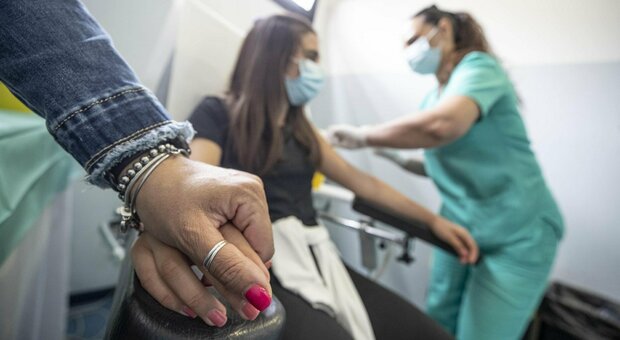
L'agenzia europea Ema ribadisce la sicurezza e l'efficacia di tutti i vaccini anti Covid approvati finora.
Segnalare sempre gli eventuali effetti avversi che dovessero presentarsi dopo il vaccino contro Covid-19. È una necessità ribadita dalla Coalizione internazionale delle autorità regolatorie (International Coalition of Medicines Regulatory Authorities, Icmra), in un appello congiunto lanciato insieme all'Organizzazione mondiale della sanità (Oms) per rafforzare la fiducia nei vaccini contro il coronavirus pandemico. «Icmra e Oms - informa l'Agenzia europea del farmaco Ema, parte dell'Icmra - esortano gli operatori sanitari non solo a segnalare diligentemente gli eventi avversi che osservano nei loro pazienti, ma anche a incoraggiare le persone vaccinate a segnalare immediatamente eventuali effetti collaterali che potrebbero verificarsi. Ciò aiuta le autorità regolatorie a valutare ogni possibile collegamento con i vaccini - precisa l' Ema - e a garantire che questi prodotti vengano utilizzati nel modo più sicuro».
La mortalià scende quando si fanno i vaccini. È un dato importantissimo da non dimenticare.
📊SESTO RAPPORTO #ISS-#ISTAT SU #COVID19 E MORTALITÀ
— Istituto Superiore di Sanità (@istsupsan) June 10, 2021
➡️ Nei primi 4 mesi del 2021 1.867.940 positivi (46% su totale casi da inizio pandemia)
🔎Dati👇https://t.co/tdoBEjkvMo@istat_it
#Covid19italia pic.twitter.com/BbPRc2nYFU
Riportiamo il comunicato ICMRA dello scorso 7 maggio in cui si spiega come devono essere trattati i dati sugli studi clinici e in cosa consistono i meccanismi di trasparenza che ne guidano la pubblicazione.
Un mese fa circa L'ICMRA (Coalizione internazionale delle autorità regolatorie) e l'OMS avevano emesso un conunicato congiunto per chiedere all'industria farmaceutica di fornire un ampio accesso ai dati clinici per tutti i nuovi farmaci e vaccini (che siano approvati in modo completo o condizionato, in caso di uso di emergenza o respinti). «I rapporti degli studi clinici - si legge nella nota - dovrebbero essere pubblicati senza la redazione di informazioni riservate per motivi di interesse prioritario per la salute pubblica».
Queste informazioni, spiegavano ICMRA e OMS insieme, servono per «sostenere la fiducia del pubblico nei vaccini».
«Il primo beneficio è la fiducia del pubblico. I regolatori aprono le loro decisioni allo scrutinio pubblico dimostrando fiducia nel loro lavoro. Un altro vantaggio è il possibile controllo dell'integrità dei dati, una necessità scientifica e un must etico. I dati devono essere robusti, esaustivi e verificabili, attraverso la revisione tra pari. L'integrità dei dati non ha prezzo. Decisioni normative sbagliate, prese su dati selezionati o inaffidabili, influenzeranno i pazienti che riceveranno quel farmaco», scrivevano ancora ICMRA e OMS.
«La mancanza di accesso pubblico alle prove negative è stata identificata come una fonte di bias, che indebolisce le conclusioni delle revisioni sistematiche e fornisce un falso senso di rassicurazione sulla sicurezza o l'efficacia del farmaco. La pubblicazione dei dati permette alla scienza di avanzare più velocemente, evitando la ripetizione di prove inutili e lo spreco di risorse (umane e finanziarie). Questo porta anche benefici migliorando l'efficienza dei programmi di sviluppo e riducendo sia i costi che i tempi di sviluppo. La pubblicazione dei dati permette anche analisi secondarie (e meta-analisi) che hanno un obiettivo diverso o complementare. Molti enti pubblici hanno reso l'accesso aperto un requisito perché i dati sono un bene comune. Fornire l'accesso ai dati è anche doveroso nei confronti dei partecipanti alla sperimentazione che hanno contribuito fisicamente e si sono assunti i potenziali rischi della ricerca», continua il comunicato.
Astrazeneca, l'Umbria sospende le seconde dosi per gli under 60
Vaccini, qual è meglio per i giovani? Differenze tra Astrazeneca, J&J, Pfizer e Moderna
Covid, Rt fermo a 0.68: «Tutte le regioni a rischio basso tranne la Sardegna»